Заметки



АНАЛИТИЧЕСКИЕ ЗАМЕТКИ
Мы начинаем регулярную публикацию на нашем сайте (www.cortec.ru) результатов исследований, выполненных на ЭТАА спектрометрах Квант Z нашей фирмы.
Надеемся, что предлагаемые материалы принесут Вам пользу.
Мы приветствуем любую форму обратной связи:
- Мы ответим на Ваши вопросы;
- Мы готовы помочь Вам в решении Ваших аналитических задач;
- Мы готовы опубликовать Ваши результаты.
КРИТИКУЙТЕ-СОМНЕВАЙТЕСЬ-ПРОВЕРЯЙТЕ-ПРЕДЛАГАЙТЕ
ОПРЕДЕЛЕНИЕ ЭЛЕМЕНТОВ В ОЧЕНЬ СОЛЕННЫХ РАСТВОРАХ
Кобальт
Основными поставщиками фонового поглощения в графитовой печи являются газообразные молекулы хлоридов и сульфатов щелочных и щелочноземельных металлов, а самым главным генератором фона является хлорид натрия. Концентрация хлорида натрия в природных водах обычно превышает 1 г/л. По солевому составу морская вода приблизительно на 75% состоит из хлорида натрия, а его средняя солёность мирового океана приблизительно равна 35 г/л. Одним из главных продуктов питания является хлорид натрия. Средняя концентрация натрия в человеческой крови 3.5 г/л, а общее содержание минеральных солей-0.9%. Изотонический раствор-это 0.9% (9г/л) раствор хлорида натрия в дистиллированной воде.
Зависимость поглощение света газообразными молекулами (паром) NaCl от длины волны имеет форму асимметричного колокола-с максимумом вблизи 250 нм, незначительно уменьшаясь при 190 нм и практически исчезая при 500 нм. Логично, сначала, исследовать фоновое поглощение вблизи 250 нм, например, на резонансной линии кобальта 240.7 нм.
Определение кобальта всегда выполняется в графитовой печи с пиролитическим покрытием.
При анализе растворов с высоким солесодержанием рекомендуется дозировать объем 5 мкл.
Оптимизированная программа нагрева графитовой печи для определения кобальта в растворе 10 г/л хлорида натрия представлена на рис. 1.
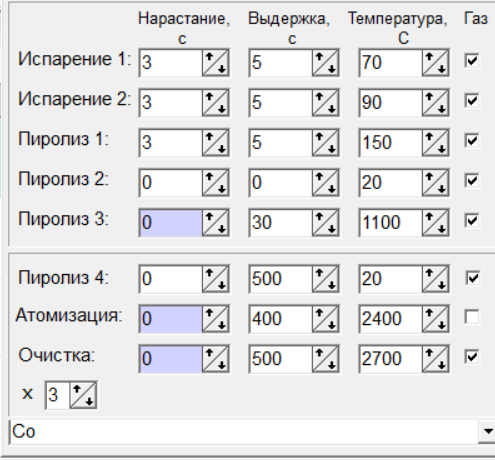
Рис. 1 Программа нагрева графитовой печи для раствора 10 г/л NaCl
Первые три стадии, ответственные за испарение воды (высушивание аликвоты) зависят от объема и не зависят от анализируемого образца. Температура атомизации 2400 С-это обычное значение для кобальта, которое, также, не зависит от анализируемого образца.
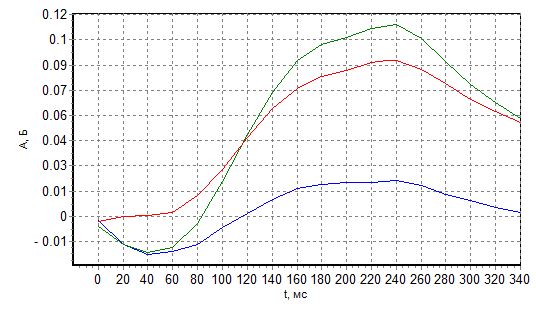
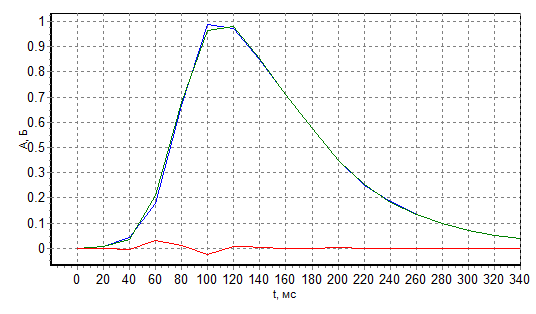
Рис. 2 Импульс атомно абсорбционности 10 мкг/л Co в дистиллированной воде. Температура пиролиза Тр=1000 С, температура атомизации Та=2400 С
Из рис. 2 следует, что аналитический сигнал-амплитуда импульса атомной абсорбционности достигается на 240 мс. Целесообразно выбрать минимальное время стадии Атомизация-400 мс, которое гарантирует регистрацию аналитического сигнала. После этого целесообразно включить высокотемпературную стадию Очистка с продувом печи потоком аргона. Укорачивание стадии Атомизация целесообразно для любой пробы, но для солевых проб это принципиально важно. Если стадию Атомизация затянуть, то пары пробы будут конденсироваться на относительно холодных торцах печи, что может привести к диафрагмированию излучения.
Для подавление фонового поглощения нужно, насколько возможно, испарить хлорид натрия. Это происходит на стадии Пиролиз 3. Параметры этой стадии являются основными инструментами борьбы с фоновым поглощением.
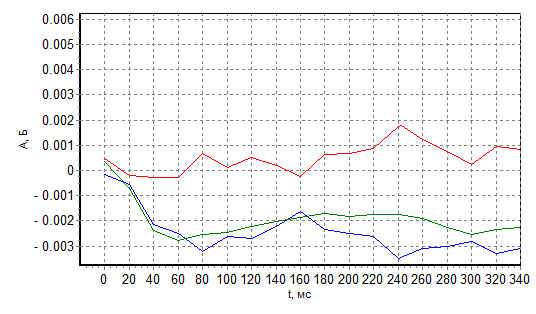
Почему выдержка равна 30 с? Из рис. 3 следует, что за 30 с 10 г/л×5 мкл=10 мкг/мкл×5 мкл=50 мкг хлорида натрия практически полностью испаряется.
a
b
Рис. 3 Сигналы испарения 50 мкг NaCl при Тп=1100 С за 30 с (а) и 5 с (б)
Почему температура пиролиза Тп=1100 С? Согласно рис. 4, именно при температуре пиролиза 1100 С 50 мкг NaCl испаряется полностью, а температуры пиролиза 1000 недостаточно для полного испарения этого количества хлорида натрия.
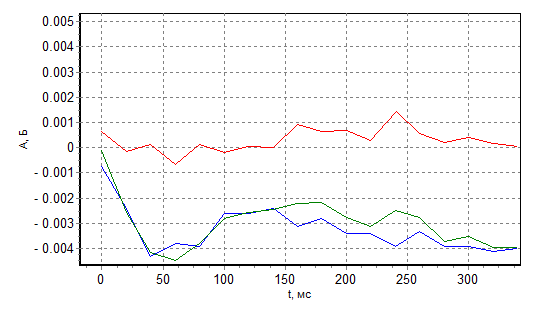
a
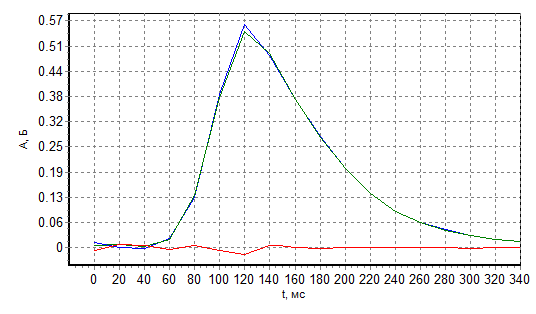
b
Рис. 4 Сигналы испарения 50 мкг NaCl при Тр=1100 С (а) и 1000 С (б)
Из рис. 4б следует, что по формальным критериям зеемановский корректор справляется с сигналом фоновой абсорбционности ≈0.57 Б. Действительно, погрешность коррекции фона, как отношение атомного и фонового сигналов, в этом измерении оказывается равной 0.00604/0.56465=0.0107, т.е. немного больше 1%. Однако, не следует обольщаться.
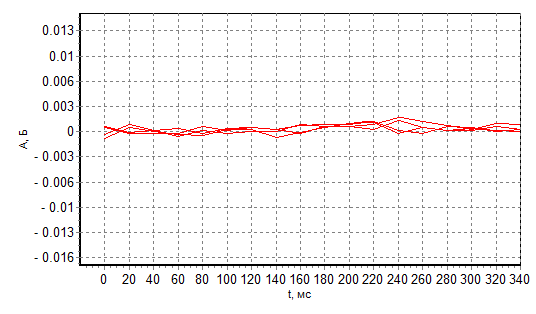
a
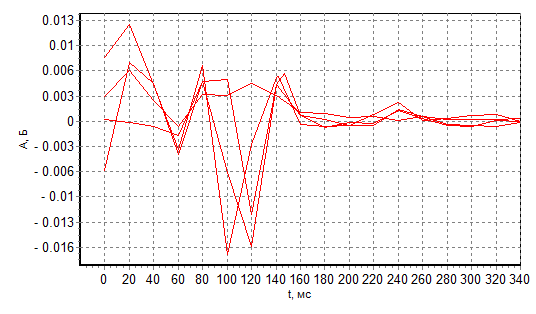
b
Рис. 5 По четыре параллельных сигнала атомной абсорбционности 50 мкг NaCl при Тр=1100 С (а) и 1000 С (б)
Рис. 5 наглядно демонстрирует, как фоновое поглощение увеличивает флуктуации сигнала атомной абсорбционности. Очевидно, что, казалось бы, скорректированное фоновое поглощение будет ухудшать и предел обнаружения элемента, и сходимость результатов измерений. Результаты определения Co в анализируемом образце (АО)-NaCl приведены на рис. 6.
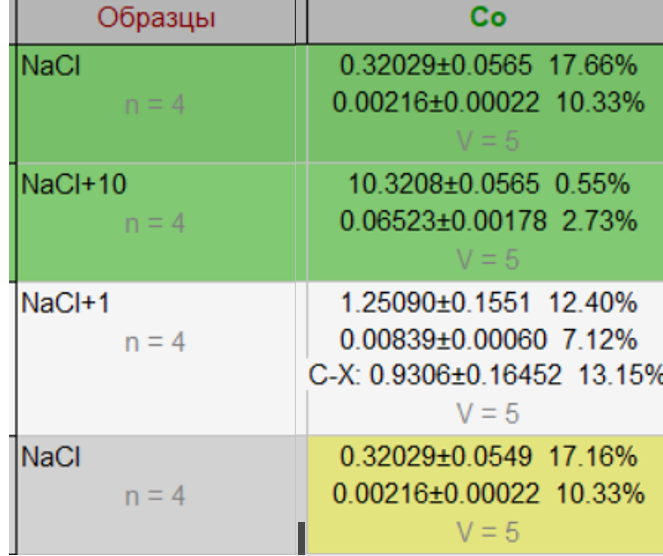
Рис. 6 Определение Co в АО-раствор 10 г/л NaCl
Измерения проводились методом стандартной добавки со постоянной функцией преобразования элемента, которая встроена в ПО. Выполняется измерения двух аналитических сигналов: для АО-NaCl и для АО с концентрационной добавкой СД элемента-NaCl+10 мкг/л Co. Программа вычисляет концентрацию элемента в АО-NaCl: (0.32±0.06) мкг/л Co и значение матричного коэффициента для АО-NaCl: k=0.0121521. Отметим, что ±0.06 мкг/л Co-это настоящее значение случайной погрешности, рассчитанной с учетом доверительной вероятности Р=0.95, числа n параллельных измерений (в приведенном примере n=4) и СКО результатов измерений.
Для установления систематической погрешности и оценки правильности выполняется определение Co АО-NaCl+1 мкг/л Co, c введенной в него концентрацией 1 мкг/л Co. Эта концентрация должна быть сравнима с измеренной концентрацией в АО-NaCl: (0.32±0.06) мкг/л Co. Для АО-NaCl+1 мкг/л Co измерена концентрация (1.25±0.16) мкг/л Co. Для АО-NaCl+1 мкг/л Co АО-NaCl является холостым образцом. С учетом результата холостого опыта концентрация в АО-NaCl+1 мкг/л Co: (0.93±0.16) мкг/л Co. Систематическая погрешность равна 1−0.93=0.07 мкг/л, меньше случайной погрешности 0.16 мкг/л. Таким образом, результат измерения введенной концентрации является правильным. Суммарная погрешность измерения концентрации 1 мкг/л Co равна √0.162+0.072=0.174642≈0.17 мкг/л. Относительная погрешность определения концентраций около 1 мкг/л Co в 10 г/л растворе NaCl равна 17%.
Концентрация 1 мкг/л является надежным пределом определения Co в 1% растворе NaCl, что следует из рис. 7, тогда как предел обнаружения Co по критерию 3σ можно оценить, как ≈3×0.033=0.1 мкг/л.
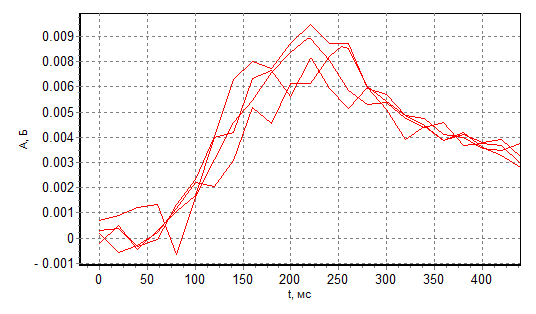
Рис. 7 АА импульсы 1 мкг/л Co в1% растворе NaCl
В качестве модельного раствора (М-раствор), имитирующего среднюю солёность морской воды 35 г/л, использовали раствор 26 г/л NaCl+5 г/л MgCl22+4 г/л Na2SO4 в дистиллированной воде.
Как и ранее дозировали 5 мкл М-раствора. Время выдержки на стадии Пиролиз 3 так же было-30 с
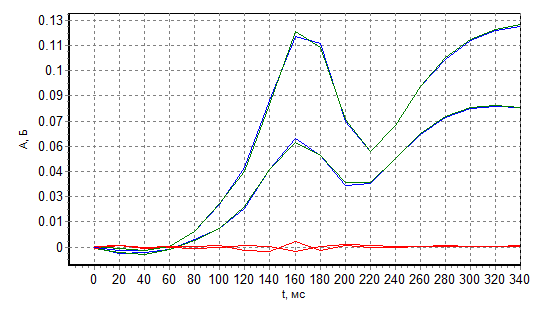
a
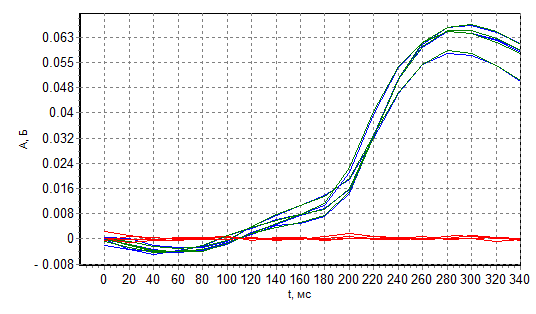
b
Рис. 8 Сигналы испарения М-раствора при Тп=1100 С (а) 1400(б)
Из рис. 3 следует, что наличие сульфата натрия в М растворе генерирует второй пик фоновой абсорбционности. Присутствие двух пиков: раннего от NaCl и позднего от Na2SO4 наблюдается при температуре пиролиза 1100 С, а при 1400 С пик от более летучего хлорида практически исчезает. Дальнейшее увеличение температуры пиролиза практически не уменьшает фоновое поглощение от менее летучего сульфата.
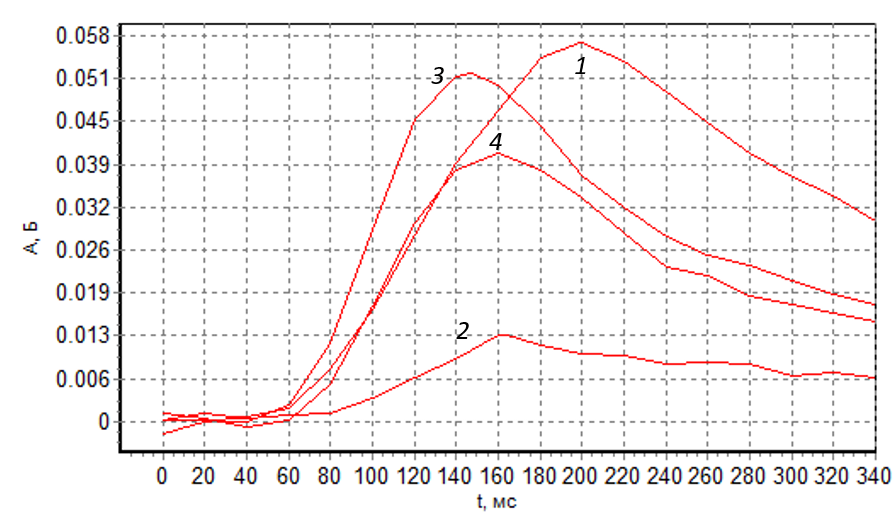
Рис. 9 АА импульсы 10 мкг/л Co дистиллированной воде (1) в М-растворе (2) и в M-растворе с добавкой 200 мг/л нитрата магния (3), в дистиллированной воде с добавкой200 мг/л нитрата магния (4)
Из рис. 9 следует, что М-раствор оказывает сильное депрессирующее влияние на Co. По сравнению с дистиллированной водой сигнал в М-растворе уменьшился в А1/A2=0.05663/0.01293≈4,4 раза. По-видимому, столь сильное влияние матрицы М-раствора обусловлено сульфатом, поскольку влияние хлорида мы не наблюдали в экспериментах с чистым NaCl. Если смириться с таким влиянием, то в М-растворе можно определить не менее 10 мкг/л Co. Но хотелось бы ниже, например, 1 мкг/л, как в 1% растворе NaCl.
Оказалось, что добавка в М-раствор 200 нитрата магния (стандартный модификатор, используемый в ЭТААС) увеличивает сигнал (3, Рис. 9-А3=0.05216) почти до того, который мы наблюдаем в дистиллированной воде (1, Рис. 9-А3=0.05663). При этом добавка нитрата магния в дистиллированную воду уменьшает сигнал до (4, Рис. 9-А4=0.04008). Это означает, что определение Co по внешней градуировке с использованием “чистых” градуировочных образцов (ГО) приведет к существенным систематической погрешности. Добавляй нитрат магния в ГО, не добавляй, значения не имеет. Погрешность останется, только изменится ее знак. Выход только один-использовать метод добавки, описанный выше.
Результаты определения Co приведены на рис. 10. Концентрация элемента в АО-М: (0.25±0.06) мкг/л Co, а значение матричного коэффициента для АО-М: k=0.0095813.
Для установления систематической погрешности и оценки правильности выполняется определение Co в АО-М+1 мкг/л, c введенной в него концентрацией 1 мкг/л Co. Эта концентрация должна быть сравнима с измеренной концентрацией в АО-М: (0.25±0.06) мкг/л Co. Для АО-М+1 мкг/л Co была измерена концентрация (1.31±0.11) мкг/л Co. Для АО-NaCl+1 мкг/л Co АО-М является холостым образцом. С учетом результата холостого опыта концентрация в АО-М+1 мкг/л Co: (1.05±0.12) мкг/л Co. Систематическая погрешность будет равна |1−1.05|=0.05 мкг/л, меньше случайной погрешности 0.12 мкг/л. Таким образом, результат измерения введенной концентрации можно признать правильным. Суммарная погрешность измерения концентрации 1 мкг/л Co равна √0.122+0.052=0.13мкг/л. Относительная погрешность определения концентраций около 1 мкг/л Co в М-растворе равна 13%.
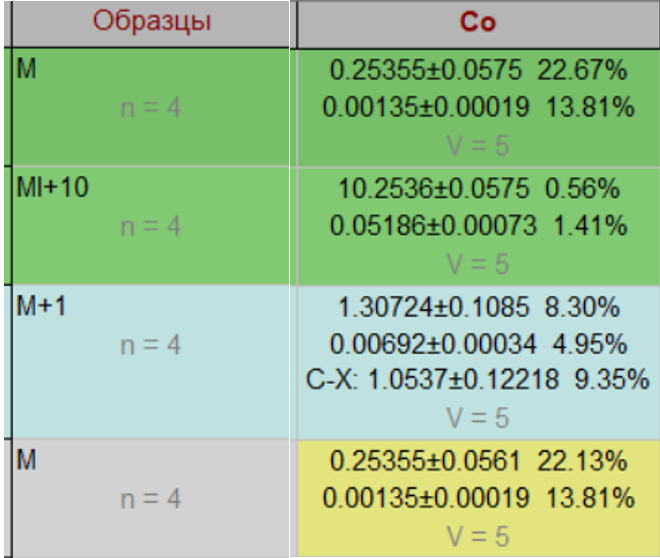
Рис. 10 Определение Co в АО-М-раствор
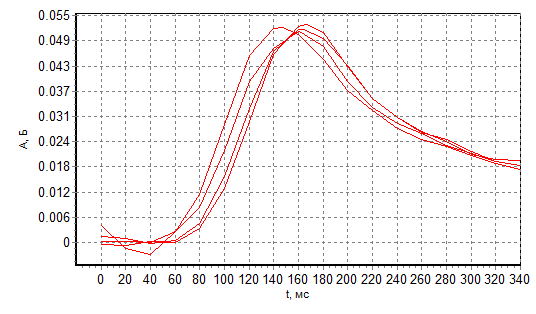
Рис. 11 АА импульсы 1 мкг/л Co вМ растворе
Если сопоставить рисунки 7,11, то пределом определения Co в М-растворе, можно принять концентрацию меньше 1 мкг/л Co.
Некоторые выводы.
Настолько ли “очень соленные” те растворы, которые мы исследовали?
Процитируем ГОСТ
Элементы-…кобальт…в диапазоне от 2 мкг/л до 5000 мкг/л. Относительная погрешность на нижней границе диапазона ±35%.
А теперь процитируем самое интересное:
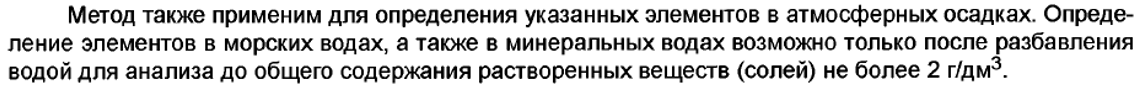
Не более 2 г/л!
А солёность М-раствора-35 г/л.
Мы не преувеличили-наши пробы действительно очень соленные.
При этом мы определяем 1 мкг/л кобальта с погрешностью ±15%.
Почувствуйте разницу!